Innovación para la Enseñanza de la Química
QSAR-3D COMO HERRAMIENTA ABSTRACCIÓN EN LA ENSEÑANZA DE LA QUÍMICA MEDICINAL
Dimas Ignacio Torres
Cátedra de Química Medicinal, Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires
E-mail: dimas_torres@hotmail.com
Recibido: 30/07/2020. Aceptado: 10/01/2020.
Resumen. Este trabajo busca analizar los beneficios y dificultades de la implementación del QSAR-3D en la enseñanza de la química medicinal. Se tratará el contexto teórico tanto del método de QSAR-3D como de las bases pedagógicas que fundamentan esta intervención educativa. Los ejes más importantes son las limitaciones actuales en la capacidad de abstracción de los alumnos y las nuevas tecnologías que habilitan plantear un enfoque novedoso en un área de suma relevancia en la química medicinal. En particular se evalúa la factibilidad de realizar un experimento computacional de forma remota. También se revelan conexiones con otras subdisciplinas de la química para remarcar su valor como contenido transversal.
Palabras clave. química medicinal, QSAR-3D, gráficos.
QSAR-3D as an abstraction tool in the education of medical chemistry
Abstract. This work seeks to analyze the benefits and difficulties of implementing QSAR-3D in the teaching of medicinal chemistry. The theoretical context of both the QSAR-3D method and the pedagogical bases that underlie this educational intervention will be discussed. The most important axes are the current limitations in the students' capacity for abstraction and the new technologies that make it possible to propose a novel approach in an area of great relevance in medicinal chemistry. In particular, the feasibility of conducting a computational experiment remotely is evaluated. Connections with other chemistry sub-disciplines are also revealed to highlight their value as cross-sectional content.
Keywords. medicinal chemistry, QSAR-3D, graphics.
INTRODUCCIÓN
La relación estructura actividad, donde se relacionan rasgos estructurales de compuestos orgánicos con su actividad biológica, es uno de los ejes principales de la química medicinal. Estas relaciones nos permiten comprender mejor cuales son los factores estructurales de los fármacos que mayor impacto y relevancia tienen en su actividad, así como también realizar predicciones cuantitativas al momento de diseñar nuevas moléculas. Esta última aplicación cobra un valor esencial al tener en cuenta el costo material que conlleva la síntesis de un compuesto químico.
Pese a la gran importancia que tiene este tema, en particular dentro del currículum de la química medicinal, su comprensión por parte de los alumnos sufre de una parcialidad agraviante. Esta dificultad se puede comprender dentro del marco teórico planteado por Johnstone (1993) y retomado por Talanquer (2011): la tríada química. Por un lado los alumnos deben comprender las características estructurales de los compuestos y su interacción con la diana biológica en el nivel sub-micro y por otro lado, tienen que poder entender el impacto en el organismo que resulta de esta interacción y los mecanismos farmacológicos que lo explican en el nivel macro. Finalmente exigimos a nuestros alumnos que conecten estos dominios materiales por un método estadístico de regresión multilineal para alcanzar un objeto abstracto que denominamos farmacóforo, el cual no existe en el mundo material sino que se ubica en un nivel simbólico.
PLANTEAMIENTO DEL PROBLEMA
La dificultad que tienen nuestros alumnos en poder realizar estas correcciones y poder aplicar estos conocimientos al diseño de fármacos ya ha sido estudiada por Talanquer (2018), en su trabajo concluye que la principal dificultad que obstaculiza el razonamiento de relaciones estructura-actividad es la fijación, en la mente de los alumnos, de los átomos o grupos funcionales de las moléculas en vez de poder ir más allá y notar las propiedades emergentes en las moléculas como un todo.
Esta dificultad puede deberse a la necesidad de enfocarse en estas propiedades estructurales al estudiar mecanismos de reacción y métodos de síntesis en cursos anteriores. La relevancia de las representaciones gráficas en la comprensión de la química orgánica fue claramente demostrado por Lorenzo y Pozo (2010). Para ayudar a los alumnos a abstraerse de las estructuras químicas, que tanto le han servido en su trayecto educativo pero que dificultan el avance en la comprensión química medicinal se plantea el uso de superficies de contorno generadas por el método de QSAR-3D como herramienta de abstracción. El objetivo de este trabajo es evaluar esta herramienta de investigación como un recurso educativo.
ANÁLISIS Y DISCUSIÓN DE LA PROPUESTA
Teoría de QSAR-3D
En la técnica clásica de QSAR desarrollada por Hansch y Fujita (1964) se toma una estructura base y se realizan modificaciones para generar un conjunto de derivados con diferentes propiedades fisicoquímicas. Estas propiedades son cuantificadas por medio descriptores (logP, sigma de Hammett, etc.) para luego implementar un modelo de regresión utilizando un parámetro de actividad biológica como variable a optimizar (logIC50, logLC50, etc.). En la Figura 1 se puede ver la estructura base y los residuos que pueden ser modificados para obtener el conjunto de entrenamiento del modelo. Esta técnica es valiosa porque es relativamente fácil de comprender desde un punto de vista procedimental pero tiene ciertas limitaciones al momento de comprender las necesidades estructurales para obtener un compuesto biológicamente activo. Éstas se presentan al momento de pedirles a nuestros alumnos que apliquen las conclusiones sacadas del modelo obtenido a compuestos con estructuras ligeramente semejantes a las que se encontraban dentro del conjunto inicial. Esto se debe a la fijación de los alumnos hacia los fragmentos constitutivos de una molécula comentada anteriormente por Talanquer (2018).
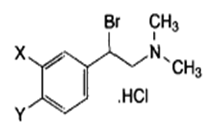
Figura 1. Estructura base para plantear modificaciones en un estudio de QSAR. Imagen extraída de Kubinyi (1997)
En la década de 1980, con el advenimiento de los métodos computacionales, una nueva aproximación al problema de las relaciones estructura-actividad fue desarrollada. Esta metodología consiste en tomar la estructura tridimensional de las moléculas y enmarcarlas en una grilla, discretizando el espacio en un número finito de elementos, para luego calcular el campo de fuerza correspondiente a cada sector como se muestra en la Figura 2.

Figura 2. Grilla que encuadra la estructura tridimensional de una estructura para discretizar el espacio en donde se desea calcular los campos de fuerza. Imagen extraída de Kubinyi (1997)
Estos vectores eran luego tratados estadísticamente para obtener factores espaciales característicos por medio de un análisis de componentes principales y luego correlacionados con la actividad biológica (lo que se denomina regresión por componentes principales o RCP). Pese al interés teórico de esta estrategia no fue hasta 1988, cuando se lanzó al mercado un software que automatiza todo este procedimiento (reemplazando el método de componentes principales por cuadrados mínimos parciales), fue que obtuvo una amplia aceptación dentro del ámbito académico e industrial (Cramer, Patterson y Bunce, 1988).
Implementación de la propuesta educativa
Dado que la mayores dificultades que se encuentran al momento de plantear un trabajo práctico computacional son de índole procedimental, una nueva plataforma desarrollada por un grupo de la universidad de Roma es de suma relevancia en la factibilidad de esta propuesta. La plataforma www.3d-qsar.com integra todos los pasos del desarrollo de un modelo QSAR-3D en un solo software con una interfaz amigable. Los desarrolladores brindan varios casos de su implementación junto con las publicaciones que lanzaron al mundo académico como información complementaria (Ragno y col, 2020). Esto reduce considerablemente tanto la curva de aprendizaje de los alumnos como el tiempo de planificación del docente.
En este caso particular se planteó el uso de un conjunto de derivados quinoxalínicos, desarrollados por integrantes de la cátedra donde me desempeño, como inhibidores de la transcriptasa reversa del virus del HIV. Esta selección permite el uso de los conocimientos desarrollados en la cátedra para acercar a los alumnos al trasfondo de la investigación académica, así como también poner en juego el interés por una patología sumamente relevante en la medicina contemporánea. Por último dado que la plataforma permite el acceso al software por cualquier persona con acceso a internet esta propuesta es consecuente con la actual condición social en la que nos coloca la actual pandemia mundial.
Dificultades y ventajas pedagógicas del QSAR-3D
Pese a que a primera vista el método 3D puede parecer más complejo que su contraparte bidimensional, un estudio más detallado puede cambiar esta impresión inicial. En primer lugar, el uso de campos de fuerza ya forma parte del currículum actual de la química medicinal al explicar las simulaciones por dinámica molecular. En segundo lugar, el concepto subyacente la RCP es similar al proceso de selección del mejor modelo de regresión de QSAR-2D donde debe evitar el uso de descriptores con alta correlación y seleccionar los que tengan mayor impacto en la respuesta. De esta forma la RCP puede ser vista como una formalización matemática de las reglas heurísticas que enseñamos actualmente a nuestros alumnos.
Una vez sofocada la aprehensión inicial frente a este método podemos pasar a considerar sus ventajas. La principal de ellas es que permite captar las propiedades globales de las moléculas en estudio liberándonos de los elementos que las conforman como se puede ver en la Figura 3 (Ballante y Ragno, 2012). En esta imagen se presentan las superficies de contorno calculadas por un método de QSAR-3D que marcan los sitios de mayor energía usando una sonda de carbono.
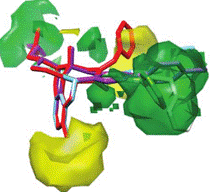
Figura 3. Mapas de contorno de impedimento estéticos de agonistas opioides calculados por QSAR-3D. Imagen extraída de Ballante y Ragno (2012).
La segunda ventaja, y la que con mayor énfasis quiero destacar, son los mapas de contornos que representan los coeficientes que se obtienen tras el proceso de regresión entre los campos de fuerza y las propiedades biológicas que pueden verse en la Figura 4. Dado que los elementos usados en la regresión tiene una distribución espacial también lo tienen los coeficientes obtenidos, de esta manera se puede visualizar las zonas más relevantes para la actividad biológica de la forma más gráfica posible. Estos mapas de contorno son la imagen más cercana al concepto abstracto de un farmacóforo que somos capaces de mostrar a nuestros alumnos y en este punto fundamental es donde radica el valor pedagógico que tiene el QSAR-3D para ayudar a nuestros alumnos a alcanzar el nivel simbólico de la química planteado por Johnstone (1993).

Figura 4. Mapas de contorno que representan los coeficientes de regresión del modelo de PLS distribuidos espacialmente, que representa el farmacóforo en QSAR-3D. Imagen extraída de Ballante y Ragno (2012).
CONCLUSIONES E IMPLICACIONES
Los elementos sobre los que querría reflexionar son de índole pedagógicos. Para empezar deseo remarcar el valor conceptual de poder presentar a nuestros alumnos un medio gráfico por el cual pueden representarse la idea abstracta de un farmacóforo. Esta idea fue la que me motivó a buscar las diferentes formas de representación que se usan actualmente para referirse a este concepto central en la química medicinal.
Retomando el marco teórico de Johnstone (1993), se puede ver cómo el QSAR en general forma el tercer pilar que permite al alumno conectar los niveles sub-micro y macro que se interrelacionan tan estrechamente en el diseño de fármacos. La ventaja que tiene su versión tridimensional es que ayuda a superar las dificultades encontradas por Talanquer (2018) en la visión fragmentaria que tienen los alumnos al momento de encontrarse con esta nueva forma de ver la química.
Finalmente querría remarcar las posibles relaciones transdisciplinares con otras áreas de la química que pueden darse con la implementación del QSAR-3D. Por un lado el uso de RCP es de uso habitual en la quimiometría, una herramienta que está en auge dentro de la química analítica y que tiene grandes exponentes dentro de la comunidad científica argentina. Por otro lado los conceptos de relación estructura-actividad están siendo aplicados a problemas fundamentales como los son el desarrollo de nuevas formas de almacenamiento de energía y en la elucidación de mecanismos de reacción electroquímicos (Robinson y Sigman, 2020).
REFERENCIAS BIBLIOGRÁFICAS
Ballante, F. y Ragno, R. (2012). 3-D QSAutogrid/R: An alternative procedure to build 3-D QSAR models. Methodologies and applications. Journal of chemical information and modeling, 52(6), 1674–1685. https://doi.org/10.1021/ci300123x
Cramer, R. D., Patterson, D. E. y Bunce, J. D. (1988). Comparative molecular field analysis (CoMFA). 1. Effect of shape on binding of steroids to carrier proteins. Journal of the American Chemical Society, 110(18), 5959–5967. https://doi.org/10.1021/ja00226a005
Hansch, C., Fujita, T. (1964). p-σ-π Analysis. A Method for the Correlation of Biological Activity and Chemical Structure. Journal of the American Chemical Society, 86(8), 1616–1626. https://doi.org/10.1021/ja01062a035
Johnstone, A. H. (1993). The development of chemistry teaching: a changing response to a changing demand. Journal of Chemical Education, 70(9), 701-705. https://doi.org/10.1021/ed070p701
Kubinyi, H. (1997). QSAR and 3D QSAR in drug design Part 1: methodology. Drug Discovery Today, 2(11), 457-467. https://doi.org/10.1016/S1359-6446(97)01079-9
Lorenzo, M. G. y Pozo, J. I. (2010). La representación gráfica de la estructura espacial de las moléculas: eligiendo entre múltiples sistemas de notación. Cultura y Educación, 22(2), 231-246. https://doi.org/10.1174/113564010791304555
Ragno, R., Esposito, V., Di Mario, M., Masiello, S., Viscovo, M. y Cramer, R. (2020). Teaching and Learning Computational Drug Design: Student Investigations of 3D Quantitative Structure–Activity Relationships through Web Applications. Journal of Chemical Education, 97(7), 1922-1930. https://doi.org/10.1021/acs.jchemed.0c00117
Robinson, S. y Sigman, M. (2020). Integrating Electrochemical and Statistical Analysis Tools for Molecular Design and Mechanistic Understanding. Accounts of Chemical Research, 53(2), 289–299. https://doi.org/10.1021/acs.accounts.9b00527
Talanquer, V. A. (2011). Macro, Submicro, and Symbolic: The many faces of the chemistry “triplet”. International Journal of Science Education, 33, 179 - 195. https://doi.org/10.1080/09500690903386435
Talanquer, V. A. (2018). Progressions in reasoning about structure-property relationships. Chemical Education Research and Practice, 19, 998-1009. https://doi.org/10.1039/C7RP00187H