La Educación en la Química en Argentina y en el Mundo
A cien años de la entrega de los Premios Nobel de Química: 1925
EL BRILLO DE UN MUNDO SUBMICROMÉTRICO
Luciano Benedini
Universidad Nacional del Sur, Dpto. de Biología, Bioquímica y Farmacia- INQUISUR-CONICET- Bahía Blanca, Buenos Aires, Argentina
Email: lbenedini@uns.edu.ar
Recibido: 18/06/2025. Aceptado: 30/06/2025.
Resumen. Este artículo celebra los 100 años del Premio Nobel en Química otorgado a Richard Adolf Zsigmondy en 1925, destacando su contribución al estudio de los coloides y la invención del ultramicroscopio. Su trabajo permitió visualizar partículas menores a 200 nm, revelando fenómenos como el efecto Tyndall y el movimiento browniano, fundamentales para la comprensión de sistemas coloidales. El texto recorre cómo estos avances sentaron las bases de múltiples desarrollos actuales en las industrias farmacéutica, cosmética, alimentaria y tecnológica. Además, se abordan los conceptos clave de emulsiones, micelas, niosomas y cristales líquidos, con aplicaciones que van desde la limpieza doméstica hasta la liberación controlada de fármacos. A un siglo de su reconocimiento con el Nobel, este es un momento propicio para recuperar el legado de Zsigmondy en la enseñanza de la química y valorar el impacto duradero de la ciencia básica.
Palabras clave. Richard Zsigmondy, química coloidal, ultramicroscopio, sistemas coloidales, emulsiones y micelas.
The Glow of the Microscopic World
Abstract. This science communication article commemorates the 100th anniversary of the 1925 Nobel Prize in Chemistry awarded to Richard Adolf Zsigmondy, recognizing his contributions to colloidal chemistry and the invention of the ultramicroscope. His work enabled the observation of particles smaller than 200 nm, unveiling key phenomena such as the Tyndall effect and Brownian motion—both essential to understanding colloidal systems. The article explores how these discoveries laid the foundation for a wide range of current applications in the pharmaceutical, cosmetic, food, and technology industries. Key concepts such as emulsions, micelles, niosomes, and liquid crystals are explained, showing their relevance from everyday cleaning to advanced drug delivery. One hundred years after his Nobel recognition, this is a timely opportunity to recover Zsigmondy’s legacy in chemistry education and to reflect on the lasting impact of basic scientific research.
Keywords. Richard Zsigmondy, colloidal chemistry, ultramicroscope, colloidal systems, emulsions and micelles.
RICHARD ADOLF ZSIGMONDY Y LOS COLOIDES
En nuestra vida cotidiana, las características que nos hacen únicos como especie interaccionan con un entorno que cambia a un ritmo cada vez más rápido. Desde las épocas de los faraones egipcios, hasta el siglo XVI con la invención del microscopio, la percepción de lo más diminuto de nuestro entorno no pudo ser analizado ni reinterpretado sustancialmente. Esto no quiere decir que los alquimistas egipcios no hayan trabajado con sustancias elementales, así como hoy se encuentran definidos, microestructuras o con nanoestructuras fascinantes, solo que no contaban con la tecnología para evidenciarlos. Si bien en el siglo XVI fue cuando se comenzó a descubrir que para la formación de una estructura que se veía como única, había pequeñas contribuciones que hacían posible que estas existan como tales. Recién en el siglo XVII es cuando se empezó a desentrañar cómo eran los aportes de estas pequeñas porciones para que nuestros objetos de estudio tomaran forma. Los primeros hitos que revelaron estructuras diminutas sucedieron en el siglo XVII, en los cuales Anton van Leeuwenhoek le mostró al mundo la existencia de organismos unicelulares y Robert Hooke la presencia de una unidad diferenciada dentro de una estructura mayor a la que llamó célula. Los hechos más sobresalientes de la química ocurrieron recién en el siglo XIX con Dalton y más tarde con Thompson cuando demostraron la naturaleza ultramicroscópica de la materia, aunque sin poder “ver” esas pequeñísimas unidades constitutivas. La conjunción de la utilización de dispositivos para ver estructuras muy pequeñas con la comprensión de la naturaleza o estructuras químicas nos lleva a uno de los científicos más importantes de la historia, el químico, Richard Adolf Zsigmondy (Viena 1865-Gotinga 1929).
Zsigmondy se interesó por la ciencia desde temprana edad, estudió en la Facultad de Medicina de Viena y en la Universidad Politécnica de Viena. Luego se mudó a Múnich donde se doctoró en química orgánica. En 1893 se graduó como profesor en la Escuela Superior Técnica de Graz donde ejerció como docente. El estudio sobre colores lustrosos en vidrio y porcelana llevó al científico a profundizar en la química de los coloides. Esta especialización le permitió trabajar en la fábrica de vidrio Schott und Genossen de Jena hasta 1900 cuando dejó su puesto y se dedicó exclusivamente a la investigación científica. Durante este período, descubrió cómo preparar hidrosoles de oro de forma reproducible y en 1903 desarrolló el ultramicroscopio de rendija junto con el físico Henry Friedrich Wilhelm Siedentopf de la empresa Zeiss. Por estos dos hechos, Zsigmondy es conocido, hoy en día, como uno de los padres de química coloidal junto con Thomas Graham. En 1907, Zsigmondy fue nombrado profesor y director del Instituto de Química Inorgánica de la Universidad de Gotinga, hasta su jubilación en febrero de 1929. En 1925, después de la primera guerra mundial, Zsigmondy recibió el Premio Nobel de Química por su trabajo sobre la naturaleza heterogénea de las “soluciones” coloidales y específicamente por el desarrollo del ultramicroscopio (Nobel Prize Outreach AB, 2023).
Lo revolucionario del diseño del ultramicroscopio diseñado por Zsigmondy, fue que permitió determinar la presencia de partículas menores a 200 nm mediante la implementación de espejos e iluminación lateral. En los microscopios convencionales de esa época se lograba una resolución que no llegaba a los 200 nm y a través de este tipo de iluminación se lograron ver partículas de hasta 5–10 nm evitando el deslumbramiento proporcionado por iluminación inferior (Masters, 2020). Este tipo de iluminación, perpendicular al eje de observación, generaba dos efectos clave:
- Efecto Tyndall: las partículas coloidales (demasiado pequeñas para ser vistas directamente) dispersaban la luz, apareciendo como puntos brillantes contra un fondo oscuro. Este efecto fue descubierto por John Tyndall en 1869 y correspondía a dispersión lumínica “el brillo” de partículas menores a 1μm (1000 nm) en dispersiones de fluidos (aire y líquido).
- Movimiento browniano: esto permitió medir el tamaño y forma a través de este fenómeno.
Observando partículas de oro coloidal, Zsigmondy, describió este último fenómeno confirmando que el movimiento browniano dependía de la viscosidad y el tamaño de las partículas que estaba observando. Esto llevó a Einstein, en 1905, a formular la relación entre el coeficiente de difusión y el “tamaño” de la partícula, que actualmente es conocida como la ecuación de Stokes-Einstein (ecuación 1), donde D es el coeficiente de difusión; KB, la constante de Boltzmann; T, la temperatura absoluta; η, la viscosidad del fluido y rH, el radio hidrodinámico de la partícula incluyendo su capa de hidratación (o sea, no es solo el “tamaño”).
![]() (ecuación 1)
(ecuación 1)
Esta ecuación es clave en la medición del tamaño de partículas que se determinan a través de técnicas como la dispersión dinámica de luz (Dynamic Light Scattering, DLS) (Stetefeld, McKenna y Patel, 2016).
Mediante el estudio de las partículas de oro coloidal se explicó por qué el vidrio rojo rubí, con el que los egipcios construyeron copas ceremoniales y parte de los pigmentos en vasijas, se veía color rojo por la adición de oro nano particulado. En principio, se genera una dispersión de la luz producida por las nanopartículas que generan el “brillo” descripto por Tyndall.
Ahora, el color rojo. Si era oro ¿por qué se veía rojo? Este color es debido a la formación de un plasmón. Es un efecto de cambio de color generado por la reflexión o dispersión de la luz roja (longitudes de onda más largas, ~600–700 nm) por absorción de otra luz de longitud de onda diferente. Esto produce una oscilación colectiva de electrones libres en la superficie de un metal cuando interactúan con la luz. Entonces, en las nanopartículas metálicas (de 1–100 nm) se produce una oscilación de electrones que dispersan luz de colores específicos, dependiendo del tamaño, forma y material de las partículas. Lo interesante es que la aparición del color rojo nos está hablando de un determinado tamaño cercano a 30 nm y a tamaños mayores (60 nm) los colores pueden variar a púrpura o azul (Kelly, Coronado, Zhao, y Schatz, 2003).
LOS COLOIDES CIEN AÑOS DESPUÉS
¿Cuál es la relevancia que tiene hoy haber llegado a descubrir las propiedades de estas nanopartículas de oro coloidal? ¿Tienen alguna aplicación? La verdad es que sí, para nombrar una, Sun y col. (2024) han desarrollado de una tira inmunocromatográfica basada en oro coloidal para detectar la IgA secretoria específica de la proteína espiga de la cepa Omicron del SARS-CoV-2 en los fluidos del revestimiento de la mucosa nasal, o sea, un test de diagnóstico.
Con esto, podemos visualizar una asociación entre Zsigmondy, los egipcios, las nanopartículas de oro y la importancia del estudio de ciencia básica como piedra fundamental para el diseño de nuevas tecnologías 100 años después.
Pero no hemos hablado aún de cuál es la importancia de haber diseñado un ultramicroscopio para determinar si un sistema puede o no ser homogéneo. ¿Es importante reconocer si un sistema es homogéneo o no? Ya sabemos que los sistemas coloidales no son homogéneos, entonces ¿qué es un sistema coloidal? ¿qué ejemplos conocemos? ¿cuál es la importancia que tienen?
En respuesta a la primera pregunta: si no supiéramos que un sistema coloidal no es homogéneo, no sabríamos que gracias a la naturaleza diferencial de las fases que lo componen, pueden llegar a absorber suciedad limpiando una superficie. Estamos hablando, en este ejemplo puntual, de una dispersión micelar de detergentes (o surfactantes, aunque los términos no pueden ser estrictamente intercambiables). Los sistemas coloidales más relevantes tienen surfactantes en su composición y a continuación me enfocaré principalmente en estos. Por lo tanto, ahora vamos a seguir respondiendo las preguntas para aclarar un poco más este tema.
Los sistemas coloidales son sistemas heterogéneos formados por dos fases bien definidas. A diferencia de los sistemas homogéneos, como una disolución no saturada de NaCl en agua, aquí se pueden diferenciar dos componentes. Entonces podemos decir que tienen una fase que se dispersa en otra con límites bien marcados. A la fase dispersa se le puede llamar discontinua y a la dispersante continua. Estas pueden ser de naturaleza muy diversa pero siempre cumpliendo la regla de que la fase discontinua debe poseer un tamaño de partícula individual de 1 a 1000 nm (1μm). Por lo visto, hemos empezado a describir sistemas submicrométricos, de otra manera, nanométricos. La fase dispersante (o externa) puede ser sólida (un metal o aleación), semisólida (gel) o líquida (una solución) y la dispersa (o interna) líquida o gaseosa. Obviamente, y como no podía ser de otra manera, hay excepciones.
En la industria alimenticia, farmacéutica, cosmética y electrónica aparecen numerosos ejemplos de sistemas coloidales. Las tres primeras muestran muchísimos puntos de contacto donde entrarían algunos tipos de emulsiones y espumas. Entre la segunda y la cuarta hay un ejemplo que se roba todas las miradas, los cristales líquidos. LCD es el acrónimo de liquid crystal display (pantalla de cristal líquido) y es la base tecnológica de la cual surgen las pantallas planas. En el campo farmacéutico, más precisamente, como sistemas transportadores de drogas (Drug Delivery Systems, DDSs), forman un mundo aparte. Dentro de los DDSs líquidos y semisólidos encontramos innumerables formulaciones que responden a la clasificación de sistemas coloidales (Figura 1).
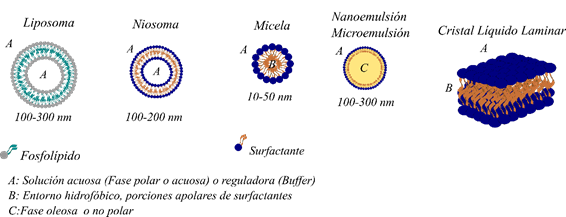
Figura 1. Sistemas coloidales basados en sistemas con surfactantes.
¿Quién no se ha aplicado una crema alguna vez? Las cremas son emulsiones, un tipo particular de sistema coloidal, donde ambas fases son líquidas, siendo la interna menor a 1000 nm. Pueden presentarse como directas, cuando la fase externa es acuosa y la interna oleosa, o reversa/inversa cuando sucede lo contrario. Lo interesante, es que se encuentran estabilizadas por una membrana de surfactante o más de uno.
Los surfactantes son moléculas que tienen la capacidad dual de disolverse en un medio acuoso (o más polar) y uno no acuoso o bien oleoso (menos polar). Por lo tanto, estas moléculas se encuentran orientadas entre las dos fases disminuyendo la tensión interfacial (entre las fases).
Las emulsiones cuando poseen un tamaño de partícula grande (mayores a 1000 nm) se denominan groseras o gruesas, pero hay otras que se llevan toda la atención en el campo farmacéutico que son las micro y las nanoemulsiones (ME y NE). Lo que resulta interesante es que por sus prefijos se puede tender a caer en una confusión y pensar que las ME tienen tamaños de fase interna en el orden del micrómetro y las NE en el orden del nanómetro y esto es falso. Tanto ME como las NE tienen tamaños muy parecidos en el orden de los ~100-200 a ~300-400 nm. Entonces acá surge una pregunta, ¿cómo las diferenciamos? Principalmente por el método de preparación y por su comportamiento frente a las condiciones del entorno. Ambas emulsiones pueden ser directas o reversas/inversas, pero las ME son termodinámicamente estables, o sea, se producen espontáneamente cuando se cumplen determinadas condiciones de proporción entre los solventes que forman las fases, concentración de surfactantes (las ME también necesitan co-surfactantes) y temperatura. La NE no son termodinámicamente estables, sino cinéticamente estables, o sea, no se producen espontáneamente, sino que es necesario desarrollarlas bajo estricto mezclado de sus componentes y aplicando una alta energía (como la proporcionada por un homogeneizador de alta presión) o mediante un cambio controlado de temperatura (temperatura de inversión de fase). Las NE son sistemas muy atractivos como DDSs ya que las condiciones del entorno no afectan a su estabilidad (dentro de ciertos límites) por lo que pueden ser diluidas muchas veces y seguir manteniendo su tamaño de partícula (Benedini y Messina, 2022a).
Existen unos sistemas más novedosos que se llaman autoemulsionables (se conocen en inglés como Self Emulsifying Drug Delivery Systems, SEDDSs), donde los componentes de la fase interna, los surfactantes y los agentes farmacéuticos activos (principios activos o drogas) se mezclan y se incorporan en un dispositivo de administración, como una cápsula, pero sin utilizar una fase externa. Cuando la cápsula es ingerida, se degrada, libera el contenido y el mismo fluido estomacal forma la fase externa de la emulsión que puede ser nano o micro según como haya sido diseñada (Singh, Bandopadhyay, Kapil, Singh, y Katare, 2009).
Existen otros sistemas coloidales más simples basados en surfactantes, las micelas o sistemas micelares y los niosomas. Debido a su capacidad dual los surfactantes se orientan en la interfase. En el caso de las micelas, las cabezas polares se orientan hacia el disolvente polar que, si es externo, se llaman micelas directas (como las emulsiones) o reversas/inversas en caso contrario. A diferencia de las emulsiones, en las micelas directas no hay un solvente no polar (oleoso) en su interior, sino que el interior no polar está formado por las colas hidrocarbonadas o porción apolar del surfactante. Esto les permite disolver o transportar fármacos liposolubles, en los casos de formulaciones farmacéuticas, pero también funcionar como detergentes capturando la suciedad y arrastrarla sin que se redeposite en la superficie. O sea, ¡el poder de las micelas lo observamos en la vida cotidiana mientras lavamos los platos! Los niosomas tienen la misma naturaleza que las soluciones micelares, con la diferencia de que en lugar de poseer una capa de surfactantes en la interfase poseen dos. Digamos que son como un liposoma, que en lugar de estar formado por una doble capa de fosfolípidos como si fuera una membrana celular, están formadas por surfactantes no-fosfolipídicos conteniendo una solución acuosa en su interior (Figura 1) (Benedini y Messina, 2022b).
Es importante remarcar que, para mejorar la estabilidad de los liposomas se utilizan otras moléculas en general liposolubles como el colesterol. En sintonía con los liposomas, se encuentran unas vesículas que poseen una composición similar a estos (con fosfolípidos), pero provienen de las células eucariotas: los exosomas y las vesículas extracelulares. Estas vesículas prometen ser los nuevos DDSs, sin embargo, sus métodos de aislamiento siguen siendo muy costosos (D'Elía, Gravina, Benedini, y Messina, 2024). Finalmente, los cristales líquidos (CL) son los sistemas coloidales menos difundidos en su concepto, aunque el acrónimo LCD, cuando hablamos de pantallas de dispositivos, es algo muy común. Los CL son llamados también mesofases. Esto se debe a que poseen propiedades intermedias entre sólidos y líquidos. Entonces, poseen un cierto orden espacial de los sólidos (cristalinos), por los que las moléculas del surfactante o agregados de ellas (pueden ser micelas) ocupan un lugar particular en el espacio formando algo parecido a una red cristalina y adicionalmente, asumen la capacidad de fluir de una fase líquida. Se han descripto numerosas mesofases pero principalmente se dividen en dos grupos: los termotrópicos, que se forman por variación de la temperatura; y los liotrópicos, que se forman por variación de la concentración del surfactante. Como siempre, hay algunos matices que hacen más difícil esta clasificación. Estas estructuras forman parte de nuevas formas de vehiculización de fármacos, sobre todo, de los liposolubles (Benedini y Messina, 2021). En la figura 1 se muestra un ejemplo de un cristal líquido laminar (liotrópico).
REFLEXIÓN FINAL
Hoy en día los sistemas coloidales siguen despertando el mismo entusiasmo que el siglo XIX. En aquellos tiempos, se estudiaron con el objetivo de descifrarlos y hoy, usando técnicas y conceptos basados en aquellos descubrimientos, los utilizamos, adaptamos, y modificamos con objetivos científicos básicos, pero también asumiendo que forman un grupo excelente de herramientas para mejorar tanto el tratamiento como el diagnóstico de enfermedades. Los conocimientos en sistemas coloidales también se aplican a otras industrias como la petroquímica. Traer a la actualidad conceptos que comenzaron a tomar forma hace más de 100 años y que se aplican al desarrollo de sistemas complejos, como son los sistemas coloidales, me hace recordar un concepto descripto por Friedrich Nietzsche, entre otros autores, el cual refiere a que la originalidad radica en cómo se reinterpreta lo ya conocido.
AGRADECIMIENTOS
El autor agradece a la Universidad Nacional del Sur (UNS), Bahía Blanca, Argentina (UNS-PGI 24/Q131) y al Concejo Nacional de Investigaciones Científicas y Técnicas de la República Argentina (CONICET).
REFERENCIAS BIBLIOGRÁFICAS
Benedini, L. A. y Messina, P. V. (2021). Nanodevices for Facing New Challenges of Medical Treatments: Stimuli-Responsive Drug Delivery Systems. Systematic Reviews in Pharmacy, 12(2), 43–64. https://doi.org/10.31838/srp.2021.2.5
Benedini, L. y Messina, P. (2022a). Lipid-based nanocarriers for drug delivery: microemulsions versus nanoemulsions. En: A. K. Nayak, M. S. Hasnain, T. M. Aminabhavi y V. P. Torchilin (Eds.). Systems of Nanovesicular Drug Delivery, (pp. 39–53). Elsevier. https://doi.org/10.1016/B978-0-323-91864-0.00001-2
Benedini, L. y Messina, P. (2022b). Proniosomes and niosomes for enhanced drug delivery. En: A. K. Nayak, M. S. Hasnain, T. M. Aminabhavi y V. P. Torchilin (Eds.). Systems of Nanovesicular Drug Delivery (pp. 115–128). Elsevier. https://doi.org/10.1016/B978-0-323-91864-0.00005-X
D’Elía, N. L., Gravina, A. N., Benedini, L. A. y Messina, P. V. (2024). A commentary: harnessing vesicles power with new scenes of membrane-based devices for drug delivery. BIOCELL, 48(10), 1401–1403. https://doi.org/10.32604/biocell.2024.055512
Kelly, K. L., Coronado, E., Zhao, L. L. y Schatz, G. C. (2003). The Optical Properties of Metal Nanoparticles: The Influence of Size, Shape, and Dielectric Environment. The Journal of Physical Chemistry B, 107(3), 668–677. https://doi.org/10.1021/jp026731y
Masters, B. R. (2020). Richard Zsigmondy and Henry Siedentopf’s Ultramicroscope. En: B. R. Masters (Ed.), Superresolution Optical Microscopy (pp. 165–172). Springer. https://doi.org/10.1007/978-3-030-21691-7_10
Nobel Prize Outreach AB. (2023). Richard Zsigmondy – Biographical. NobelPrize.Org. https://www.nobelprize.org/prizes/chemistry/1925/zsigmondy/biographical/
Singh, B., Bandopadhyay, S., Kapil, R., Singh, R. y Katare, O. P. (2009). Self-Emulsifying Drug Delivery Systems (SEDDS): Formulation Development, Characterization, and Applications. Critical Reviews in Therapeutic Drug Carrier Systems, 26(5), 427–451. https://doi.org/10.1615/CritRevTherDrugCarrierSyst.v26.i5.10
Stetefeld, J., McKenna, S. A. y Patel, T. R. (2016). Dynamic light scattering: a practical guide and applications in biomedical sciences. Biophysical Reviews, 8(4), 409–427. https://doi.org/10.1007/s12551-016-0218-6
Sun, B., Chen, Z., Feng, B., Chen, S., Feng, S., Wang, Q., Niu, X., Zhang, Z., Zheng, P., Lin, M., Luo, J., Pan, Y., Guan, S., Zhong, N. y Chen, L. (2024). Development of a colloidal gold-based immunochromatographic assay for rapid detection of nasal mucosal secretory IgA against SARS-CoV-2. Frontiers in Microbiology, 15. https://doi.org/10.3389/fmicb.2024.1386891