La Educación en la Química en Argentina y en el Mundo
EL PREMIO NOBEL DE QUÍMICA 2023
Luz Lastres
Universidad de Buenos Aires
Email: klastres@gmail.com
Recibido: 27/11/2023. Aceptado: 15/12/2023.
Resumen. Se presenta una traducción al español de artículos difundidos en la página web del Premio Nobel. En esta traducción se incluye información referente a las investigaciones realizadas por Moungi Bawendi, Louis Brus y Alexei Ekimov para el desarrollo y síntesis de puntos cuánticos, por las cuales fueron distinguidos por el Premio Nobel en Química en 2023.
Palabras clave. Premio Nobel, puntos cuánticos, síntesis, caracterización.
The Nobel Prize in Chemistry 2023
Abstract. A Spanish translation of articles disseminated on the Nobel Prize website is presented. This translation includes information regarding the research conducted by Moungi Bawendi, Louis Brus, and Alexei Ekimov for the development and synthesis of quantum dots, for which they were awarded the Nobel Prize in Chemistry in 2023.
Keywords. Nobel Prize, quantum dots, synthesis, characterization.
Traducción al español de información contenida en:
Science Editors: Peter Brzezinski, Heiner Linke, Johan Åqvist, the Nobel Committee for Chemistry
Text: Ann Fernholm
Translation: Clare Barnes
Illustrations: Johan Jarnestad
Editor: Alicia Hegner
©The Royal Swedish Academy of Sciences
La Real Academia Sueca de Ciencias ha decidido conceder el Premio Nobel de Química 2023 a Moungi G. Bawendi, Instituto de Tecnología de Massachusetts (MIT), Cambridge, MA, EE. UU., Louis E. Brus, Universidad de Columbia, Nueva York, NY, EE. UU. y Alexei I. Ekimov, Nanocrystals Technology Inc., Nueva York, NY, EE. UU.
“por el descubrimiento y síntesis de puntos cuánticos”

Moungi G. Bawendi, nacido en 1961 en París, Francia. Doctorado 1988 de la Universidad de Chicago, IL, EE. UU. Profesor del Instituto de Massachusetts de Tecnología (MIT), Cambridge, MA, EE. UU.

Louis E. Brus, nacido en 1943 en Cleveland, OH, EE. UU. Doctorado en 1969 por la Universidad de Columbia, Nueva York, NY, EE. UU. Profesor de la Universidad de Columbia, Nueva York, NY, EE. UU.

Alexei I. Ekimov, nacido en 1945 en la antigua URSS. Doctorado en 1974 por el Instituto Físico-Técnico Ioffe, San Petersburgo, Rusia. Anteriormente científico jefe de Nanocrystals Technology Inc., Nueva York, NY, EE. UU.
Le agregaron color a la nanotecnología
Moungi G. Bawendi, Louis E. Brus y Alexei I. Ekimov reciben el Premio Nobel de Química 2023 por el descubrimiento y desarrollo de puntos cuánticos. Estas pequeñas partículas tienen propiedades únicas y ahora difunden su luz desde pantallas de televisión y lámparas LED. Catalizan reacciones químicas. y su luz clara puede iluminar el tejido tumoral para un cirujano.
"Toto, tengo la sensación de que ya no estamos en Kansas", es una cita clásica de la película El mago de Oz. Dorothy, de doce años, se desmaya en su cama cuando un poderoso tornado arrasa su casa, pero cuando la casa vuelve a aterrizar y ella sale por la puerta, con su perro Toto en brazos, todo ha cambiado. De repente se encuentra en un mundo mágico en tecnicolor.
Si un tornado encantado entrara en nuestras vidas y redujera todo a nanodimensiones, es casi seguro que quedaríamos tan asombrados como Dorothy en la tierra de Oz. Nuestro entorno sería deslumbrantemente colorido y todo cambiaría. Nuestros pendientes de oro brillarían de repente azules, mientras que el anillo de oro en nuestro dedo brillaría con un rojo rubí. Si intentáramos freír algo en la cocina de gas, la sartén podría derretirse. Y nuestras paredes blancas –cuya pintura contiene dióxido de titanio– comenzarían a generar muchas especies reactivas oxigenadas.

Figura 1. Los puntos cuánticos nos han brindado nuevas oportunidades para crear luz coloreada.
El tamaño importa en la nanoescala
En el nanomundo, las cosas realmente se comportan de manera diferente. Una vez que se empieza a medir el tamaño de la materia en millonésimas de milímetro, comienzan a ocurrir fenómenos extraños (efectos cuánticos) que desafían nuestra intuición. Todos los premios Nobel de Química de 2023 han sido pioneros en la exploración del nanomundo. A principios de los años 1980, Louis Brus y Alexei Ekimov lograron crear– independientemente uno de otro – puntos cuánticos, que son nanopartículas tan pequeñas que los efectos cuánticos determinan sus características. En 1993, Moungi Bawendi revolucionó los métodos de fabricar puntos cuánticos, lo que hace que su calidad sea extremadamente alta, un requisito previo vital para su uso en la nanotecnología actual.
Gracias al trabajo de los galardonados, la humanidad ahora puede utilizar algunas de las propiedades peculiares del nanomundo. Los puntos cuánticos se encuentran actualmente en productos comerciales y se utilizan en muchos ámbitos científicos y disciplinas, desde la física y la química hasta la medicina, pero nos estamos adelantando. Vamos a descubrir los antecedentes del Premio Nobel de Química 2023.

Figura 2. Un punto cuántico es un cristal que a menudo consta de unos pocos miles de átomos. En términos de tamaño, tiene la misma relación. a una pelota de fútbol que una pelota de fútbol tiene al tamaño de la Tierra.
Durante décadas, los fenómenos cuánticos en el nanomundo fueron sólo una predicción
Cuando Alexei Ekimov y Louis Brus produjeron los primeros puntos cuánticos, los científicos ya sabían que podrían, en teoría, tener características inusuales. En 1937, el físico Herbert Fröhlich había ya predicho que las nanopartículas no se comportarían como otras partículas. Exploró las consecuencias teóricas de la famosa ecuación de Schrödinger, que muestra que cuando las partículas se vuelven extremadamente pequeñas hay menos espacio para los electrones del material. A su vez, los electrones –que son a la vez ondas y partículas – se comprimen entre sí. Fröhlich se dio cuenta de que esto daría lugar a cambios drásticos en las propiedades del material.
Los investigadores quedaron fascinados con esta idea y, utilizando herramientas matemáticas, lograron predecir numerosos efectos cuánticos dependientes del tamaño. También trabajaron para intentar demostrarlos en la realidad, pero era más fácil decirlo que hacerlo porque necesitaban esculpir una estructura que fuera aproximadamente un millón de veces más pequeño que la cabeza de un alfiler.
Pocas personas pensaron que se podrían utilizar los efectos cuánticos
Aun así, en la década de 1970, los investigadores lograron crear dicha nanoestructura. Usando un tipo de haz molecular crearon una capa nanofina de material de recubrimiento encima de un material a granel. Una vez completada, pudieron demostrar que las propiedades ópticas del recubrimiento variaban dependiendo de cuan delgado era, una observación que coincidía con las predicciones de la mecánica cuántica.
Este fue un gran avance, pero el experimento requirió tecnología muy avanzada. Los investigadores necesitaban tanto un vacío ultra alto como temperaturas cercanas al cero absoluto, por lo que pocas personas esperaban que los fenómenos de la mecánica cuántica podrían llegar a tener un uso práctico. Sin embargo, de vez en cuando la ciencia ofrece lo inesperado y, esta vez, el punto de inflexión se debió a los estudios de un antiguo invento: el vidrio coloreado.
Una sola sustancia puede dar al vidrio diferentes colores
Los hallazgos arqueológicos más antiguos de vidrio coloreado datan de hace varios miles de años. Los vidrieros se abrieron camino para comprender cómo se puede producir vidrio en todos los colores del arco iris.
Agregaron sustancias como plata, oro y cadmio, luego jugaron con diferentes temperaturas para producir hermosos tonos de vidrio.
En los siglos XIX y XX, cuando los físicos comenzaron a investigar las propiedades ópticas de luz, se puso en práctica el conocimiento de los vidrieros. Los físicos podrían utilizar vidrio coloreado para filtrar longitudes de onda de luz seleccionadas. Para optimizar sus experimentos, empezaron a producir vidrio ellos mismos, lo que condujo a importantes ideas. Una cosa que aprendieron fue que una sola sustancia podría resultar en vidrio de colores completamente diferentes. Por ejemplo, una mezcla de seleniuro de cadmio y sulfuro de cadmio podía hacer que el vidrio se volviera amarillo o rojo; en cuál se convertía dependía de cuánto se calentaba el vidrio fundido y cómo se enfriaba. Finalmente, también pudieron demostrar que los colores provenían de partículas que se formaban dentro del vidrio y que el color dependía del tamaño de las partículas.
Este era más o menos el estado del conocimiento a finales de los años 1970, cuando uno de los laureados de este año, Alexei Ekimov, recién graduado de doctorado, comenzó a trabajar en el Instituto Estatal S. I. Vavilov de Óptica en lo que entonces era la Unión Soviética.
Alexei Ekimov mapea los misterios del vidrio coloreado
El hecho de que una sola sustancia pudiera dar lugar a vidrios de diferentes colores interesó a Alexei Ekimov, porque en realidad es ilógico. Si pintas un cuadro en rojo cadmio, siempre será rojo cadmio, a menos que mezcle otros pigmentos. Entonces, ¿cómo podría una sola sustancia producir vidrio de diferentes colores?
Durante su doctorado, Ekimov estudió semiconductores, componentes importantes de la microelectrónica. En este campo, los métodos ópticos se utilizan como herramientas de diagnóstico para evaluar la calidad de los materiales semiconductores. Los investigadores iluminan el material y miden la absorbancia. Esto revela de que sustancias está hecho el material y qué tan bien ordenada está la estructura cristalina.
Ekimov estaba familiarizado con estos métodos, por lo que comenzó a utilizarlos para examinar vidrios coloreados. Después de algunos experimentos iniciales, decidió producir sistemáticamente vidrio teñido con cloruro de cobre. Calentó el vidrio fundido a un rango de temperaturas entre 500°C y 700°C, variando el tiempo de calentamiento de 1 hora a 96 horas. Una vez que el vidrio se enfrió y endureció, lo radiografió.
Los rayos dispersos mostraron que se habían formado pequeños cristales de cloruro de cobre dentro del vidrio y que el proceso de fabricación afectaba el tamaño de estas partículas. En algunas de las muestras de vidrio tenían sólo unos dos nanómetros, en otros eran hasta 30 nanómetros
Curiosamente, resultó que la absorción de luz del vidrio se veía afectada por el tamaño de las partículas. Las partículas más grandes absorbieron la luz de la misma manera que lo hace normalmente el cloruro de cobre, pero cuanto más pequeñas eran las partículas, más azul era la luz que absorbían. Como físico, Ekimov estaba bien familiarizado con las leyes de la mecánica cuántica y rápidamente se dio cuenta de que había observado un efecto cuántico dependiente del tamaño (Figura 3).
Esta fue la primera vez que alguien logró producir deliberadamente puntos cuánticos: nanopartículas que causan efectos cuánticos dependientes del tamaño. En 1981, Ekimov publicó su descubrimiento en una revista científica soviética, pero fue de difícil acceso para los investigadores del otro lado de la Cortina de Hierro. Por lo tanto, otro Premio Nobel de Química de este año, Louis Brus, desconocía el descubrimiento de Alexei Ekimov cuando, en 1983, fue el primer investigador del mundo en descubrir los efectos cuánticos dependiente del tamaño en partículas que flotan libremente en una solución.
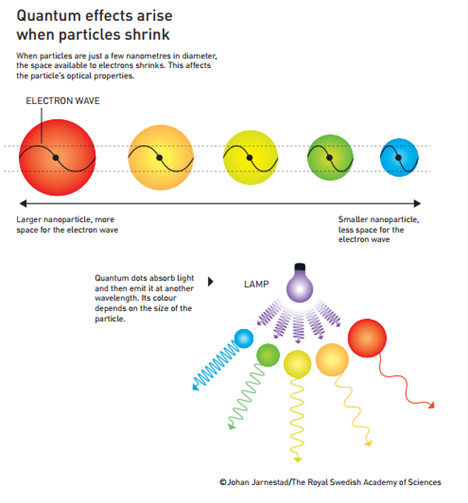
Figura 3. Surgen efectos cuánticos cuando las partículas se encogen. Cuando las partículas tienen sólo unos pocos nanómetros de diámetro, el espacio disponible para los electrones se reduce. Esto afecta las propiedades ópticas de la partícula. Los puntos cuánticos absorben luz y luego la emiten en otra longitud de onda. Su color depende del tamaño de la partícula.
Brus demuestra que las extrañas propiedades de las partículas son efectos cuánticos
Louis Brus trabajaba en los Laboratorios Bell en Estados Unidos, con el objetivo a largo plazo de hacer que las reacciones químicas se produzcan usando energía solar. Para lograrlo, utilizó partículas de sulfuro de cadmio, que pueden capturar la luz y luego utilizar su energía para impulsar reacciones. Las partículas estaban en una solución y Brus las hizo muy pequeñas porque esto le daba un área más grande en la que las reacciones químicas podrían tener lugar; cuanto más se muele un material, mayor será la superficie que quedará expuesta a sus alrededores.
Mientras trabajaba con estas diminutas partículas, Brus notó algo extraño: sus propiedades ópticas cambiaban después de haberlas dejado en la mesa del laboratorio por un tiempo. Supuso que esto podría deberse a que las partículas habían crecido, por lo que para confirmar sus sospechas produjo partículas de sulfuro de cadmio que tenían apenas unos 4,5 nanómetros de diámetro. Brus luego comparó las propiedades ópticas de estas partículas recién formadas con las de las partículas más grandes, que tenían un diámetro de aproximadamente 12,5 nanómetros. Las partículas más grandes absorbieron luz en las mismas longitudes de onda que el sulfuro de cadmio generalmente lo hace, pero las partículas más pequeñas tuvieron una absorción que se desplazó hacia el azul (Figura 3).
Al igual que Ekimov, Brus comprendió que había observado un efecto cuántico dependiente del tamaño. Él publicó su descubrimiento en 1983 y luego comenzó a investigar partículas formadas a partir de una variedad de otras sustancias. El patrón era el mismo: cuanto más pequeñas eran las partículas, más azul era la luz que absorbían.
La tabla periódica ganó una tercera dimensión
Aquí es donde usted puede sentirse tentado a preguntar: "¿Por qué importa si la absorbancia de una sustancia es ligeramente más hacia el azul? ¿Por qué es eso tan sorprendente?
Pues bien, los cambios ópticos revelaron que las características de la sustancia habían cambiado por completo. Las propiedades ópticas de una sustancia están gobernadas por sus electrones. Los mismos electrones también gobiernan otras propiedades de la sustancia, como su capacidad para catalizar reacciones químicas o conducir electricidad. Entonces, cuando los investigadores detectaron el cambio en la absorción, entendieron que, en principio, estaban mirando un material completamente nuevo.
Si quieres entender la magnitud de este descubrimiento, puedes imaginar que la tabla periódica de repente ganó una tercera dimensión. Las propiedades de un elemento no sólo se ven afectadas por el número de capas de electrones y cuántos electrones hay en la capa exterior, sino que, a nivel nano, el tamaño también importa. Por lo tanto, un químico que quisiera desarrollar un nuevo material tendría otro factor con el que jugar.
¡Por supuesto que esto hizo cosquillas a la imaginación de los investigadores!
Hubo solo un problema. Los métodos que Brus había utilizado para fabricar nano partículas generalmente resultaban en calidad impredecible. Los puntos cuánticos son cristales diminutos (Figura 2) y los que podían producirse en aquella época a menudo contenía defectos. También eran de diferentes tamaños. Era posible controlar cómo se formaban los cristales de modo que las partículas tuvieran un tamaño promedio determinado, pero si los investigadores quisieran todas las partículas en una solución tuvieran aproximadamente el mismo tamaño, tenían que clasificarlas después de su fabricación. Este era un proceso difícil que obstaculizó el desarrollo.
Moungi Bawendi revoluciona la producción de puntos cuánticos
Este fue un problema que el tercer Premio Nobel de Química de este año decidió resolver.
Moungi Bawendi comenzó su formación postdoctoral en el laboratorio de Louis Brus en 1988, donde realizó estudios intensivos. Se estaba trabajando para mejorar los métodos utilizados para producir puntos cuánticos. Utilizando una variedad de solventes, temperaturas y técnicas, experimentaron con una variedad de sustancias para intentar formar nanocristales bien organizados. Y los cristales estaban mejorando, pero todavía no eran lo suficientemente buenos.
Sin embargo, Bawendi no se rindió. Cuando empezó a trabajar como líder de investigación en el Massachusetts Instituto de Tecnología del MIT, continuó sus esfuerzos para producir nanopartículas de mayor calidad. Un gran avance se produjo en 1993, cuando el grupo de investigación inyectó las sustancias que formarían nanocristales en un disolvente calentado y cuidadosamente elegido. Le inyectaron la mayor cantidad de sustancias posible para saturar con precisión la solución, lo que llevó a que comenzaran a formarse simultáneamente pequeños embriones de cristal (Figura 4).
Luego, al variar dinámicamente la temperatura de la solución, Moungi Bawendi y su grupo de investigación logró cultivar nanocristales de un tamaño específico. Durante esta fase, el disolvente ayudó a dar a los cristales una superficie lisa y uniforme.
Los nanocristales que produjo Bawendi eran casi perfectos y dieron lugar a distintos efectos cuánticos. Debido a que el método de producción era fácil de usar, fue revolucionario: cada vez más químicos comenzaron a trabajar con nanotecnología y comenzaron a investigar las propiedades únicas de los puntos cuánticos.
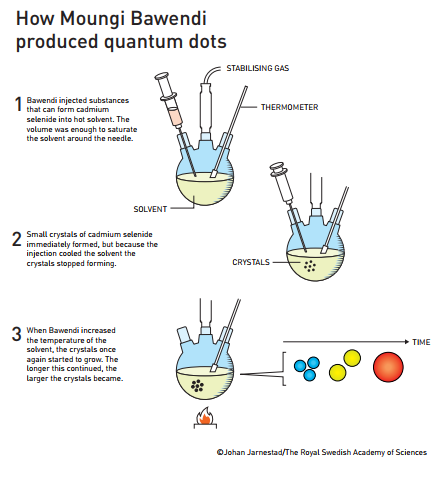
Figura 4. Como produjo puntos cuánticos Moungi Bawendi: 1.- Bawendi inyectó sustancias que pueden formar seleniuro de cadmio en solvente caliente. El volumen era suficiente para saturar el solvente alrededor de la aguja. 2.- Inmediatamente se formaron cristales de seleniuro de cadmio, pero debido a que la inyección enfriaba el solvente los cristales dejaban de formarse. 3.- Al aumentar la temperatura del solvente, nuevamente los cristales comenzaron a crecer. Cuanto más continuaba esto mayores se tornaban los cristales.
Las propiedades luminosas de los puntos cuánticos encuentran usos comerciales
Treinta años después, los puntos cuánticos son ahora una parte importante de la caja de herramientas de la nanotecnología y son encontrados en productos comerciales. Los investigadores han utilizado principalmente puntos cuánticos para crear luz coloreada. Si los puntos cuánticos se iluminan con luz azul, absorben la luz y emiten una luz de diferente color.
Modificar el tamaño de las partículas permite determinar exactamente de qué color debería brillar (Figura 3).
Las propiedades luminosas de los puntos cuánticos se utilizan en pantallas de ordenador y televisión basadas en Tecnología QLED, donde la Q significa punto cuántico. En estas pantallas, la luz azul se genera usando los diodos energéticamente eficientes que fueron reconocidos con el Premio Nobel de Física 2014. Puntos cuánticos se utilizan para cambiar el color de parte de la luz azul, transformándola en roja o verde. Esto hace posible producir los tres colores primarios de luz necesarios en una pantalla de televisión.
De manera similar, en algunas lámparas LED se utilizan puntos cuánticos para ajustar la luz fría de los diodos. La luz entonces puede volverse tan energizante como la luz del día o tan calmante como el cálido resplandor de una bombilla atenuada.
La luz de los puntos cuánticos también puede utilizarse en bioquímica y medicina. Los bioquímicos adjuntan puntos cuánticos a biomoléculas para mapear células y órganos. Los médicos han comenzado a investigar el potencial uso de puntos cuánticos para rastrear el tejido tumoral en el cuerpo. En cambio, los químicos utilizan las propiedades catalíticas de puntos cuánticos para impulsar reacciones químicas.
Por lo tanto, los puntos cuánticos están aportando el mayor beneficio a la humanidad y apenas hemos comenzado a explorar su potencial. Los investigadores creen que en el futuro los puntos cuánticos podrán contribuir a la electrónica flexible, sensores minúsculos, células solares más delgadas y quizás comunicación cuántica cifrada. Una cosa es cierta: queda mucho por aprender sobre fenómenos cuánticos sorprendentes. Entonces si hay una Dorothy de 12 años que busca aventuras, el nanomundo tiene mucho que ofrecer.